Первый препарат для лечения COVID-19 получил одобрение на продажу в ЕС

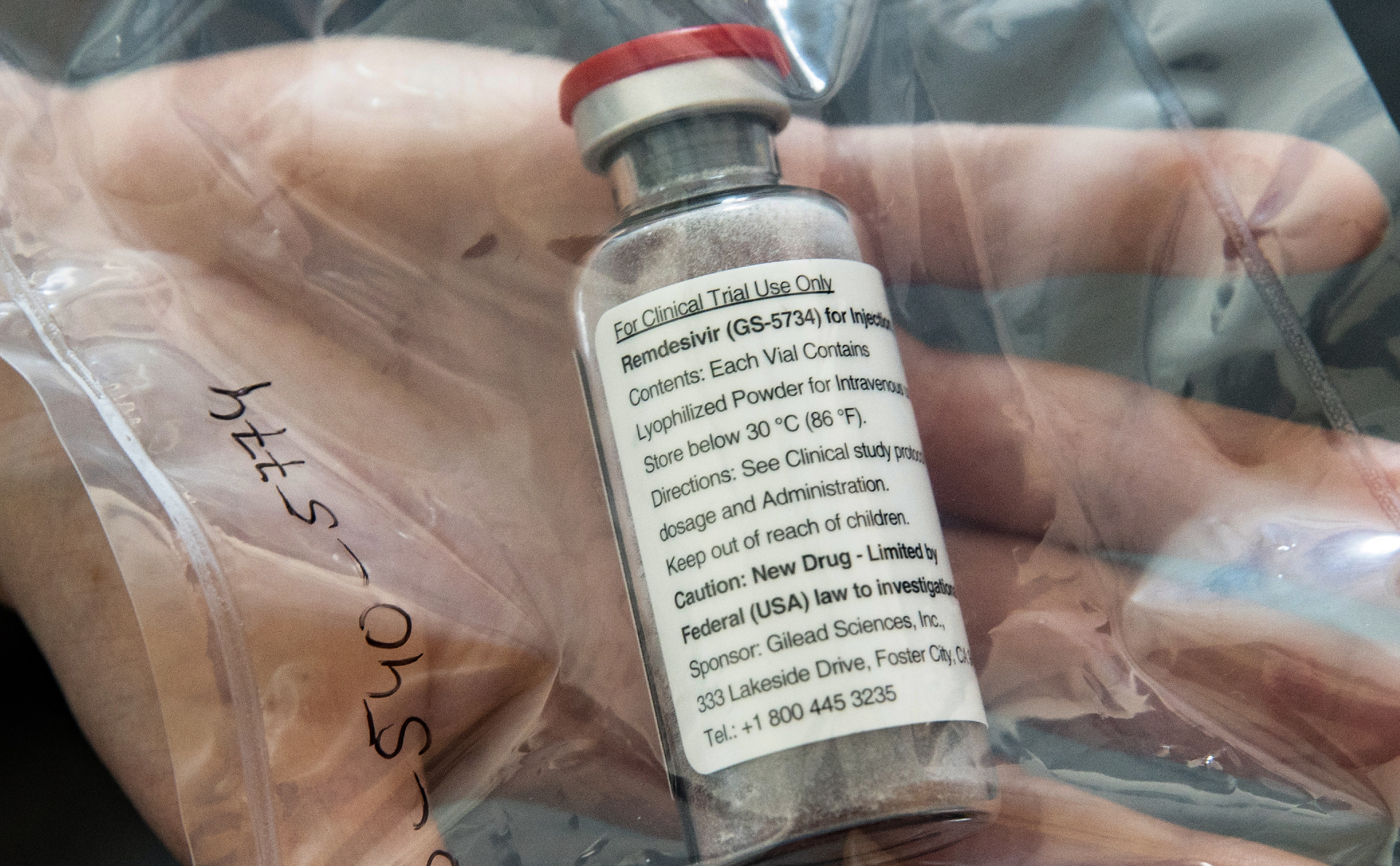
Европейское агентство по лекарственным средствам (EMA) рекомендовало предоставить условное разрешение на продажу препарата Veklury (Remdesivir, «Ремдесивир»), который можно использовать для лечения взрослых и подростков старше 12 лет с диагнозом «пневмония» и положительными тестами на коронавирус COVID-19. Об этом сообщает пресс-служба агентства.
«Ремдесивир» является первым препаратом против COVID-19, рекомендованным для получения разрешения в ЕС», — говорится в сообщении.
Условное разрешение на продажу — это один из нормативных механизмов Евросоюза для облегчения раннего доступа к лекарствам, покрывающим неудовлетворенные медицинские потребности, в том числе в чрезвычайных ситуациях, такие как пандемия коронавируса COVID-19. Такой тип одобрения позволяет EMA рекомендовать препарат для разрешения на продажу, даже если данных о его действии меньше, чем обычно требуется. Это делается, если выгода его немедленной доступности для заболевших превышает риск, связанный с тем фактом, что еще не все данные по нему доступны.
В агентстве рассказали, что комитет EMA по лекарственным средствам для человека начал оценку данных о качестве и производстве «Ремдесивира» с 30 апреля, задолго до подачи производителем заявки на получение разрешения на продажу (5 июня).
Окончательное решение по предоставлению условного разрешения, как говорится в сообщении, в основном было принято на основе данных исследования, спонсируемого американским Национальным институтом аллергических и инфекционных заболеваний (NIAID), а также нескольких других исследований. NIAID оценил эффективность применения десятидневного курса «Ремдесивира» более чем на 1 тыс. госпитализированных пациентов с COVID-19. «В целом исследование показало, что пациенты, получавшие «Ремдесивир», выздоровели примерно через 11 дней, по сравнению с 15 днями у пациентов, получавших плацебо», — отметили в агентстве.
В EMA сообщили, что на использование «Ремдесивира» действует ограничение: его можно применять только в медицинских учреждениях со стационарным режимом. Препарат применяется путем введения в вену. «Лечение должно начинаться с инфузии 200 мг в первый день, после чего ежедневно вводится по 100 мг в течение не менее четырех дней и не более девяти дней», — сообщили в агентстве.
В середине апреля канадские ученые заявили, что «Ремдесивир», который применялся для лечения лихорадки Эбола, блокирует размножение коронавируса. Они тестировали препарат для лечения ближневосточного респираторного синдрома (MERS) и атипичной пневмонии SARS-CoV, схожих по структуре РНК с нынешней коронавирусной инфекцией SARS-CoV-2. Исследователи сообщили, что результаты испытаний препарата в отношении их были практически идентичными.
В начале мая управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) выдало экстренное разрешение на использование «Ремдесивира» в США для лечения зараженных коронавирусом. За несколько дней до этого глава NIAID Энтони Фаучи говорил об успешных клинических испытаниях «Ремдесивира».
В марте в Минздраве России заявляли о том, что «Ремдесивир» находится в перечне препаратов, которые находятся на стадии клинических испытаний у пациентов с COVID-19. Тогда в ведомстве отметили, что достоверных данных об эффективности этого лекарства нет.